-
医疗器械供应链的趋势和痛点:来自一份2024年医疗器械供应链调查

供应链中断是医疗器械行业最普遍的挑战之一。这些中断可能是由多种因素引起,包括自然灾害、政治不稳定或经济衰退等。 这些问题会导致交付过程的延迟,从而延误患者护理。此外,由于原材料成本高昂和相关生产成本,供应链中断还会导致成本超支。 为确保供应链稳定,医疗器械公司需优化其供应链并制定严格的风险缓解措施。这种优化既需要战略规划,也需要战术执行。为探讨医疗技术供应链的发展趋势和当前问题,《医疗产品外包》(MPO)杂志进行了一项调查,以了解医疗器械供应链领域的实际情况。 MPO调查发现:供应商数量调整态度各异 近一半的受访者表示,他们没有计划调整合作的供应商数量,这意味着制造商相信与他们合作的供应商能满足他们的需求。而对于那些寻求改变供应商数量的公司,其原因主要包括以下几方面: 受访者观点: 质量也是选择供应商时考虑的关键要素。一位受访者希望能获得“更好的质量控制,更好地应对组件不可用的情况”,以实现“更好的产品质量和更高效的生产”。 另一位受访者补充道: 外包服务与材料类别 1.制造与辅助服务外包给第三方的制造和辅助服务类型涵盖了医疗器械制造的方方面面。最常见的包括: 制造服务,如挤出、EDM、激光加工、注塑成型、组装、包装、锻造、铸造、阳极氧化、钝化涂层和热处理。 2. 电子元件及相关服务 电子元件的外包需求也比较高,在调查对象中最常见的是: 电缆组件、柔性电路和 PCB。 3. 原材料 原材料的外包供应也很频繁。这些材料包括: 生物材料、聚合物和复合材料、纺织品、不锈钢、钛、PEEK、镍钛合金、铝和锌合金和硅胶/橡胶等。 受访者意见:供应链中的主要痛点 1. 交付周期和成本 当被调查有关其供应链的最重大痛点时,交货周期被接近一半的受访者列为主要问题。 一位受访者提到,“原型设计交付周期和成本是他们的主要挑战。“现在看来,生产数量也是同样的问题,”他们继续说道。然而,这位人士承认,“我们的公司很难合作”。 2、成本压力加剧 运输成本和交付时间是许多受访者共同关心的问题。其中一些人特别指出价格上涨和物流成本增加是主要的困扰来源。 有时,来自价格较低地区的供应商可能因物流费用的增加而丧失其竞争优势。一位受访者指出了海外供应商的一个问题: 3. 质量体系和法规复杂性 与质量体系相关的问题,以及国际规则和法规的复杂性,也是医疗器械公司面临的重大挑战,多位受访者对此提出了担忧。 受访者意见:行业普遍关切的更广泛问题 1. 并购对供应链的影响 供应链中企业并购的增多引发了广泛担忧: 2. 过度关注成本 vs 价值导向 许多受访者表达了对过于追求成本削减,而忽视与真正的合作伙伴一起交付的价值(质量、服务和供应保证),这种从合作关系转向交易关系的趋势令人担忧,在医疗器械行业中行不通。 内容来源:https://www.mpo-mag.com/the-2024-medical-device-supply-chain-survey/ 总结 医疗技术行业的供应链正在面临交货周期、物流成本、监管复杂性等诸多挑战。尽管许多企业对现有供应商网络感到满意,但围绕如何优化合作关系、平衡成本效益与可靠性的讨论愈显重要。从此次MPO的调查可看出,基于信任的合作伙伴关系的重要性,同时也呼吁应关注长期合作价值而非短期交易效率的模式。 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
智慧导管设计与加工系列三:让能量输送更加稳定的柔性电极球囊
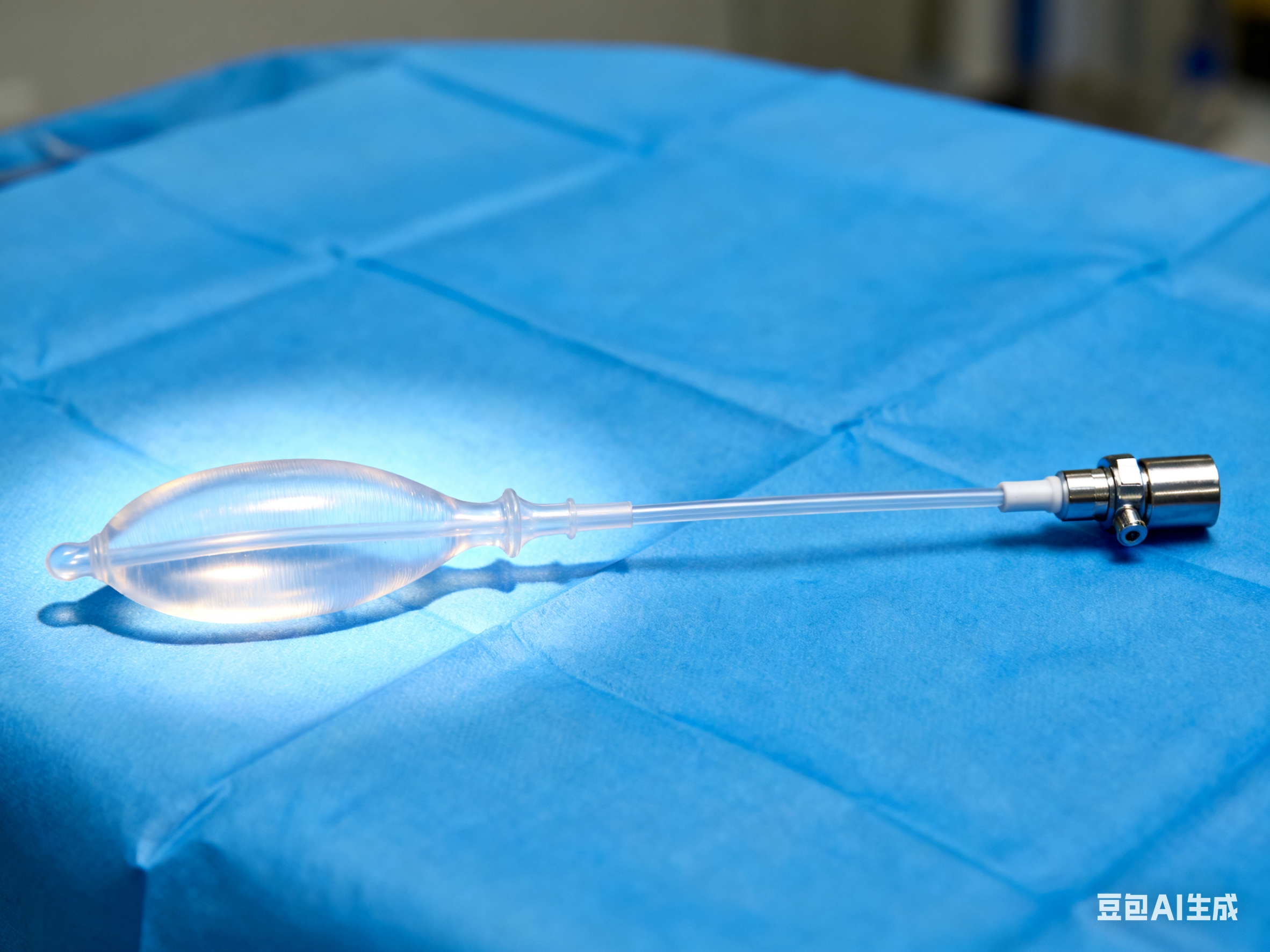
球囊是介入手术中最常用的几种耗材之一,主要的用途包括: 随着智慧导管的高速发展,球囊的特性使其更容易稳定的贴合在特定的病变位置,辅助能量输送,因此得到了越来越多的应用,比如治疗房颤的冷冻球囊导管、治疗高血压的肾动脉消融球囊导管等。 而当传感器/换能器设计在球囊表面,不管是进行温度、压力的测量,还是进行能量消融,因为可以更稳定的接近靶部位,其应用面会有更大提升,如心脏手术、泌尿外科手术、耳鼻喉科手术、神经外科手术、妇科手术等。但同时,对于导管、球囊、电极的设计和工艺也提出了更大的挑战。 对于传感器/换能器的要求 对于球囊导管的要求 索特方案 索特医疗(Salt Medical)在设计、开发和制造用于各种介入诊断和治疗的导管方面拥有丰富的经验。我们有能力整合各种诊断和治疗组件,如用于导管加固的精密编织和线圈、可调弯技术,以及用于输送、诊断和治疗的集成智慧平台,以实现广泛的临床需求。 索特团队曾协助多家射频消融、冷冻消融、超声消融、IVUS导管客户完成了诸如换能器的合作开发与供应链管理、多腔管的设计与生产、球囊囊体的设计与生产、导管的整体设计与生产、配套输送系统的设计与生产等工作,推动多款产品顺利进入临床及商业化阶段。 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
智慧导管设计与加工系列二

传统导管的活动范围和灵活性有限,主要依靠操作者的技术和经验来操纵导管尖端,以到达目标部位。可调弯导管的主要优点是可以更好地进入困难的解剖部位,提高导管在手术中的稳定性,缩短透视时间,减少病人和医生的总辐射量。 除了在电生理手术、结构性心脏病手术、外周血管手术以外,可调弯导管被用在越来越多的介入手术中,包括神经介入手术、肾动脉消融手术、肿瘤介入手术甚至关节镜等手术中。可调弯导管不仅需要精准控弯,还需要有稳定的支撑力,以及很好的抗折性、扭控性。 索特方案 材料专家:索特技术团队对包括外层热塑材料,如Nylon,Pebax(多硬度),PU等用于可控弯性能方面的材料,有着丰富的经验。可根据客户不同的需求提供最适宜的材料选择。工艺专家:索特技术团队充分理解不同加工工艺对于导管性能的影响,提供成套的金属处理(切割、焊接、打孔等)、丝线编织与卷绕、导管成型服务,以及非焊接式的控弯线多股打孔工艺。尤其擅长海波管设计与切割工艺、编织设计与工艺,充分满足导管抗折性、扭控性等性能要求。 海波管设计 编织工艺 设计专家:索特技术团队有多款全球创新导管类产品的设计开发经验,从临床目标出发,不拘泥于通用导管的材料和工艺选择,通过创新设计服务于多样化的临床需求,包括: 参考文献:Steerable catheters for minimally invasive surgery: a review and future directions. 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
智慧导管设计与加工系列一:PFA导管,关注点不只是电压

脉冲电场消融术(Pulsed Field Ablation, PFA)凭借其细胞选择特异性所带来的安全性等优势,逐步受到临床的认可。部分美国电生理专家认为,在未来一年,对PFA的使用将从如今9%增加到30%以上。PFA可能很快成为治疗房颤的主流消融技术。PFA技术的研发公司通常都会把重点放在电压、电极尺寸以及其他脉冲参数上。但是就像所有有源类导管一样,除了这些关键参数,PFA导管的整体设计也非常重要,可能会成为产品开发路上的实质性障碍。相对于通用性很高的射频消融导管,PFA导管会根据患者解剖结构做出多样化的导管设计,比如Farapulse的可变篮筐和花瓣形状的导管。这对于导管整体设计和工艺落地都提出了前所未有的挑战。包括: 等等。 索特方案 索特医疗(Salt Medical)在设计、开发和制造用于各种介入诊断和治疗的导管方面拥有丰富的经验。我们有能力整合各种诊断和治疗组件,如用于导管加固的精密编织和线圈、可调弯技术,以及用于输送、诊断和治疗的集成智慧平台,以实现广泛的临床需求。 索特团队曾协助多家射频消融、冷冻消融、超声消融、IVUS导管客户完成了诸如换能器的合作开发与供应链管理、多腔管的设计与生产、球囊囊体的设计与生产、导管的整体设计与生产、配套输送系统的设计与生产等工作,推动多款产品顺利进入临床及商业化阶段。 欢迎咨询索特医疗 爱尔兰研发中心负责人Dr. BrendanBrendan博士具有20多年医疗器械研发经验。曾历任Medtronic研发工程师以及3家欧洲知名创新器械公司研发负责人、研发VP职务,协助公司合计完成十多轮股权融资并具有完整并购退出经验。Brendan博士对血管介入创新器械的研发及工艺落地有着极强的总体设计能力,曾主导研发多款冠脉疾病、结构性心脏病、脑血管疾病创新器械,拥有十多项全球发明专利。 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
医疗器械制造的成功之路系列四:合作伙伴篇

近年来,医疗器械行业快速发展,产品研发和制造的复杂性也在逐步提高。在这一背景下,CDMO(合同设计与制造组织) 通过其专业能力和全面服务,为企业提供从概念开发到商业化生产的端到端支持,成为推动医疗器械创新的重要力量。 那么,CDMO能为医疗器械企业带来哪些价值?如何选择合适的CDMO?本文将为您详细解答。 CDMO是什么? 医疗器械合同设计与制造组织(CDMO)在整个医疗器械产品生命周期中提供端到端的服务,从最初概念的开发到设计过程的所有阶段,再到准备进行测试和临床试验的工作原型的创建。CDMO通常也提供监管支持。 另外,CDMO和CMO有明显的区别。CMO是一个合同制造组织,传统的CMO不参与对许多项目和医疗器械公司至关重要的设计和开发过程。而CDMO 在设计和开发阶段就深度参与,为企业提供更加全面和灵活的解决方案。比如包括: 无论是初创公司还是成熟的跨国企业,CDMO 都可以根据不同需求提供灵活支持。 为什么越来越多的企业选择CDMO? 选择医疗器械CDMO的主要益处包括: 选择CDMO的关键考量因素 那么,应该如何衡量一个CDMO是否值得合作呢?以下几点不可忽视: △设计开发经验 CDMO与更传统的CMO(合同制造组织)之间的关键区别在于,CDMO将拥有设计专业知识和产品开发经验。选择一个具有广泛的产品设计和开发经验的CDMO也是有益的。这包括管理完整项目的经验,处理设计的各个方面,以及增加现有设计团队开发专业组件的经验。 △行业专业知识 医疗器械行业专业化,需坚定不移地关注患者的安全、质量和合规性,因此在CDMO中,直接的医疗技术行业专业知识至关重要。 △产品专业知识 与在产品领域具有专业知识的CDMO合作是非常有益的。例如,如果您的产品是微创医疗设备,那么理想情况下,您的CDMO应该具有微创医疗设备的专业知识。 △与您的需求保持一致 您的 CDMO 应与企业的具体需求高度契合,包括: 适配性强的 CDMO 将有效降低项目风险。 △容量 容量是医疗器械项目中一个经常被忽视的组成部分,但它是必不可少的。您选择的CDMO不仅应该在今天有可用容量,而且将来也应该有可用容量。例如,您需要确信CDMO具有设计产品所需的能力,然后在准备好大规模生产时时进行生产;而您最不希望看到的是,当你即将将产品商业化时,由于产能问题而导致的延误。 △设施和设备 好的CDMO拥有“交钥匙”制造能力,拥有先进的设施和广泛的设备和资源。包括洁净室设施、先进的制造设备、最新的技术平台和熟练的员工,以及组装、包装和灭菌能力等多环节支持。 △投资策略 CDMO的投资策略也应该考虑到你的决策。比如您的CDMO是否定期投资于其能力,将决定其竞争力: 未能紧跟行业发展的 CDMO 将难以长期满足客户需求。 △解决问题的能力 通过创新设计、小型化、复杂组件和/或包含传感器等先进技术,医疗器械产品正变得越来越复杂。您的医疗器械CDMO应该具有广泛的解决问题的能力和经过验证的跟踪记录,以确保他们能够满足您的要求。 △材料专业知识 用于生产新医疗器械产品的材料对患者安全、可用性、可制造性、质量一致性、原材料可靠性以及越来越重要的可持续性至关重要。拥有材料科学专业知识的 CDMO 能够为产品质量提供额外保障。 △DFM(为制造而设计) DFM 是贯穿整个设计阶段的重要过程,确保产品能够高效、稳定地进入大规模商业化生产。DFM的目标包括减少组件的数量和最小化装配过程的复杂性。一个掌握 DFM 方法论的 CDMO 将显著提高项目的成功率。 △认证 您的医疗器械CDMO应该有一个已建立的质量管理体系(QMS)和ISO 13485认证。它还应该通过监管机构审核,并获得有效的认证。 △监管知识和支持 遵守法规是贯穿医疗器械生命周期的要求。因此,在选择CDMO时,监管知识和支持是重要的考虑因素。您的CDMO应该有质量和监管资源,为您提供所需的支持,以及完善和健全的文件控制流程。 △供应链 鉴于许多供应链在过去几年中面临的中断,供应链管理比以往任何时候都更加重要。您选择的CDMO应该具有先进和高效的供应链管理流程,包括强有力的监督,以确保供应链顺畅运行。 △持续改进…
-
医疗器械制造的成功之路系列三:持续改进篇

制造医疗器械是一项复杂的工作,单个医疗器械可能需要多个部件,其中许多部件可能非常小、复杂和精细。并且在生产过程中需要满足严格的法规要求和消毒需求。制造业的持续改进有很多定义,但基本的概念是采取一种永不停滞的策略,不断地让制造过程变得更好。 医疗器械制造的复杂性 虽然持续改进很重要,但医疗器械制造的持续改进比其他制造业的持续改进更具挑战性。这是由于患者安全和合规性的考虑。不能简单地改变一个制造过程,只因为它提高了一两个指标。任何改变都不能危及患者安全,这意味着生产工艺和程序的任何改进都必须遵循组织的质量管理体系。任何调整或变更也必须经过验证,必要时通过文件进行验证。 需改进的重点领域 在医疗器械制造中,为实现持续改进,关键在于找到那些可以优化的“切入点”: 持续改进的目标 内容参考来源:Whitepaper-Three EssentialPhases of Medical Device Manufacturing Success 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
医疗器械制造的成功之路系列二:设计转移篇

在医疗器械制造的成功之路系列上一期中,我们探讨了可制造性设计(DFM)如何通过设计优化,简化制造过程、提升效率并降低成本。而作为 DFM 的延续与实践,设计转移是将医疗器械设计引入生产的活动和过程。有效的设计转移是监管机构所要求的,但它也能控制制造成本。此外,有效的设计转移可以缩短产品上市时间,提高产品质量。 监管机构对于设计转移的要求 1. FDA的要求: 在FDA质量体系法规(21 CFR 820.30(h))中涵盖了设计转移:“每个制造商应建立和维护程序,以确保器械设计正确转化为生产规范” 。 2. ISO 13485:2016 的要求: 在 ISO 13485:2016 第 7.3.8 节中,设计转移要求明确写明::“组织应将设计和开发输出到制造的转换程序形成文件。这些程序应确保设计和开发的输出在成为最终生产规范之前以适用于生产的方式经过验证,并且生产能力能满足产品要求。转移的结果和结论应予以记录”。 3. NMPA 和 EU MDR 的要求: 虽然中国NMPA和欧盟MDR中并没有特别提到设计转移,但这些要求已经在ISO 13485的定义中得到了充分涵盖。 有效设计转移的基本组成部分 良好的做法是使用设计转移检查表来确保与转移相关的所有活动都已成功完成并记录。设计转移过程应在设计阶段尽早开始,因为应持续考虑产品的可制造性。被叫做为制造而设计(design for manufacturing),简称DFM。此外,工艺验证与设计转移密切相关,因此两者应同时进行并记录。所有与设计转移过程相关的活动都应完整地记录下来。 三阶段设计转移过程 内容参考来源:Whitepaper-Three EssentialPhases of Medical Device Manufacturing Success 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。
-
医疗器械制造的成功之路系列一:可制造性设计(DFM)篇

在医疗器械领域,每一件产品从概念到量产都必须经历复杂而精密的设计与制造过程,而可制造性设计(Design for manufacturing DFM) 就是这一过程中的核心环节。它不仅确保产品可以在目标制造成本内制造,还在保障质量、安全性及性能的同时,满足法规和可用性和患者体验。 DFM的主要目标: DFM的主要目标是在制造过程中用尽可能少的步骤使产品制造更简单、更快速。对于零件数量,设计工程师将消除或组合部件以确保用尽可能少的零件,这节省了生产和组装的时间、步骤,降低了出错的风险。除了零件减量化,零件标准化也是DFM的主要目标之一。 尽早引入DFM:事半功倍 将DFM原则纳入项目初期规划至关重要,可以有效避免后期设计修改导致的时间延误和成本增加。例如,如果设计在后期被迫调整以满足制造要求,不仅会拖延进度,还可能使项目超支。因此,尽早整合DFM,有效规避潜在风险,还能优化流程,加快产品从概念到市场的落地速度。 DFM八问:让设计经得起推敲 在设计新医疗器械产品时,DFM方法要求我们对产品和设计的各个方面提出质疑: DFM过程中需要考虑的因素 DFM后流程仍需充分优化 DFM不仅在设计阶段重要,其后续的实施也需关注以下方面: 设计转移与验证:首件检验(FAI)确保量产的一致性和可靠性,其中生产过程必须经过验证,以确保它们按规定生产产品或组件。 操作人员培训:对于参与生产和装配过程的操作人员来说,员工培训以及持续的性能监测和不断改进也是至关重要的。 供应链管理:供应链是DFM过程和决策的重要部分,这不仅包括一切顺利运行时的材料可用性,还包括出现挑战时的材料可用性、供应链的潜在瓶颈。 内容参考来源:Whitepaper-Three EssentialPhases of Medical Device Manufacturing Success 关于我们 索特医疗是一家国际化医疗器械 CDMO 公司,拥有成熟的全球研发和制造网络。公司在爱尔兰和美国设有研发中心,在亚太地区设有大型制造中心。索特专注于导管、导丝、医用内窥镜、手术机器人和其他产品领域,在心脑血管以及消化、呼吸和其他临床领域创新产品的设计、开发和生产方面积累了丰富的经验。我们利用充分协同的网络,为全球医疗设备制造商提供最具经济效益和响应速度的服务。